冠军病例|右心功能不全合并小左室终末期心衰,阜外团队植入LVAD助力新生
作者:乐乘 栏目:新闻 来源:中国经济观察网 发布时间:2026-02-25 13:46 阅读量:9460 会员投稿
内容摘要:终末期心衰,药物治疗效果欠佳,既往只能等待心脏移植,因为受限于供体的多重因素,很多患者不能得到有效救治。自从左室辅助装置(LVAD)成功上市,为广大患者群体带来了新的救治希望。然而,对于小左室、右心功能不良,叠加房颤、肾功能不全等多重难题的...
终末期心衰,药物治疗效果欠佳,既往只能等待心脏移植,因为受限于供体的多重因素,很多患者不能得到有效救治。自从左室辅助装置(LVAD)成功上市,为广大患者群体带来了新的救治希望。 然而,对于小左室、右心功能不良,叠加房颤、肾功能不全等多重难题的患者,左心室辅助装置(LVAD)的应用仍然面临很大挑战。
在本次全国LVAD病例大赛(华北赛区)中,中国医学科学院阜外医院陈凯医生分享了一例“右心功能不全合并小左室患者LVAD植入”经典病例,团队挑战“小左室+右心差”的高难度手术,成功为43岁终末期心衰患者实施无插入式LVAD(EVA-Pulsar?)植入术;术后患者心功能显著改善,完全恢复日常活动,彰显了LVAD在复杂心衰救治中的卓越价值,成功斩获本次比赛冠军。

(图:贡鸣教授为陈凯医生颁发冠军奖杯)
专家点评

王现强教授
中国医学科学院阜外医院
该病例为LMNA基因相关扩张型心肌病所致终末期心衰,核心难点在于左室偏小(LVEDD 63mm)、右心功能严重不全(TAPSE 11mm,FAC 16.6%),同时合并阵发性房颤、二尖瓣中大量反流及中度肾功能不全,属于LVAD植入的高危人群。
团队明确了肺动脉高压源于左心负荷过重,制定"左心泄压改善右心功能"的核心策略,选择无插入血管设计的EVA-Pulsar?装置,有效规避了室间隔抽吸风险。术前充分优化脏器功能、术后精准调控循环,最终实现患者心功能从IV级到完全康复的跨越,为同类复杂病例提供了标准化治疗路径。
患者基本情况与病史
患者男性,43岁,身高180cm,体重66kg,BMI 20.37kg/m2。因"发现心率减慢11年,憋喘3年,加重4个月"入院。2018年因三度房室传导阻滞植入双腔永久起搏器,2022年确诊扩张型心肌病(LMNA基因阳性),2023年心衰症状反复加重,两次住院治疗。既往无高血压、糖尿病、冠心病病史,有胆囊切除手术史。
入院诊断:扩张型心肌病、心脏扩大、二尖瓣轻中度关闭不全、三尖瓣轻中度关闭不全、心律失常(三度房室传导阻滞、起搏器植入术后、阵发性房颤、室早)、心功能IV级(NYHA分级)、肺动脉高压、肾功能不全、左肾结石、胆囊切除术后,AHA分期D期,INTERMACS 3级。
术前评估
初始评估(2025年4月3日)
实验室检查:NT-ProBNP高达26830pg/ml,肌酐228μmol/L(eGFR 29ml/(min·1.73m2),重度肾功能不全),总胆红素升高,提示多脏器功能受累。
心脏超声:左室舒张末径63mm(相对偏小),左室射血分数(LVEF)27%,TAPSE 11mm,RV-FAC 16.6%,二尖瓣中大量反流,三尖瓣少量反流,肺动脉收缩压39mmHg,提示双心功能严重受损。
循环状态:血压90/60mmHg,心率60次/分,需间断利尿及胺碘酮控制心律失常,入院后曾突发心衰发作,予米力农、去甲肾上腺素等药物后症状改善。
动态评估与优化(2025年4月3日-4月22日)
经米力农、新活素等药物治疗及漂浮导管血流动力学监测,患者病情逐步改善。
漂浮导管检查结果显示:
·2025年4月17日:肺动脉收缩压(PAPs)69mmHg,肺动脉平均压40mmHg,肺血管阻力235Woods单位,肺动脉楔入压30mmHg,心输出量3.4L/min,中心静脉压4mmHg。
·2025年4月18日(持续优化后):PAPs改善至60mmHg,肺动脉平均压35mmHg,肺血管阻力降至147Woods单位,心输出量3.8L/min。
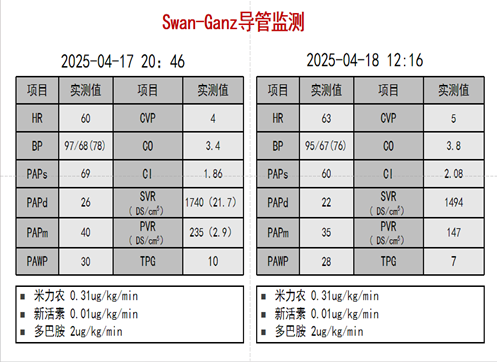
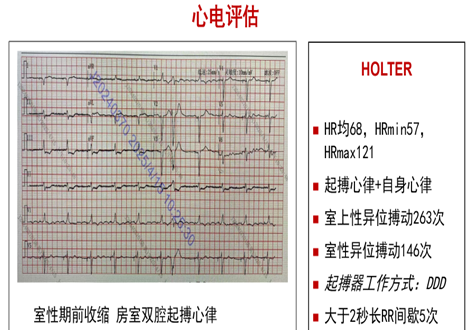
这些数据变化表明,患者的肺高压主要源于左心前负荷升高,支持通过LVAD植入实现左心减负进而改善肺循环和右心功能的治疗策略。
脏器功能改善:NT-ProBNP从26830pg/ml降至3111pg/ml,肌酐从228μmol/L降至127μmol/L(eGFR改善至55.4ml/(min·1.73m2),转为中度肾功能不全),总胆红素恢复正常,二尖瓣反流减少至中量,肺淤血明显改善。
影像学复查(2025年4月8日):冠脉CTA未见明确狭窄,全主动脉CTA提示轻度粥样硬化,升主动脉无明显钙化增厚;头颅CTA无出血或梗塞灶,排除神经系统禁忌。
系统评估:肺通气功能正常,小气道功能异常;感染指标经抗感染治疗后恢复正常;凝血功能、营养状况无特殊异常;患者依从性好,家庭支持条件佳,无明确抗凝禁忌。
综合评估:患者符合LVAD植入术适应证(终末期心衰、INTERMACS 3级、心功能IV级),经术前优化后脏器功能可逆,具备手术条件。
手术过程
患者于2025年4月23日在全麻低温体外循环下行左心室辅助装置(EVA-Pulsar?)植入术,体外循环时间74分钟,主动脉阻断时间56分钟。
·循环支持建立:采用标准体外循环路径,维持术中血流动力学稳定,避免右心负荷过重。
·左室辅助装置植入:暴露左心室心尖部,由于患者左室偏小,选择EVA-Pulsar?的无插入血管设计,在心尖处建立进流通道,避免了传统有插管式设计对左室腔体的占据,规范处理心尖后植入装置。术中设置泵速1800转/分,流量3.5L/min。
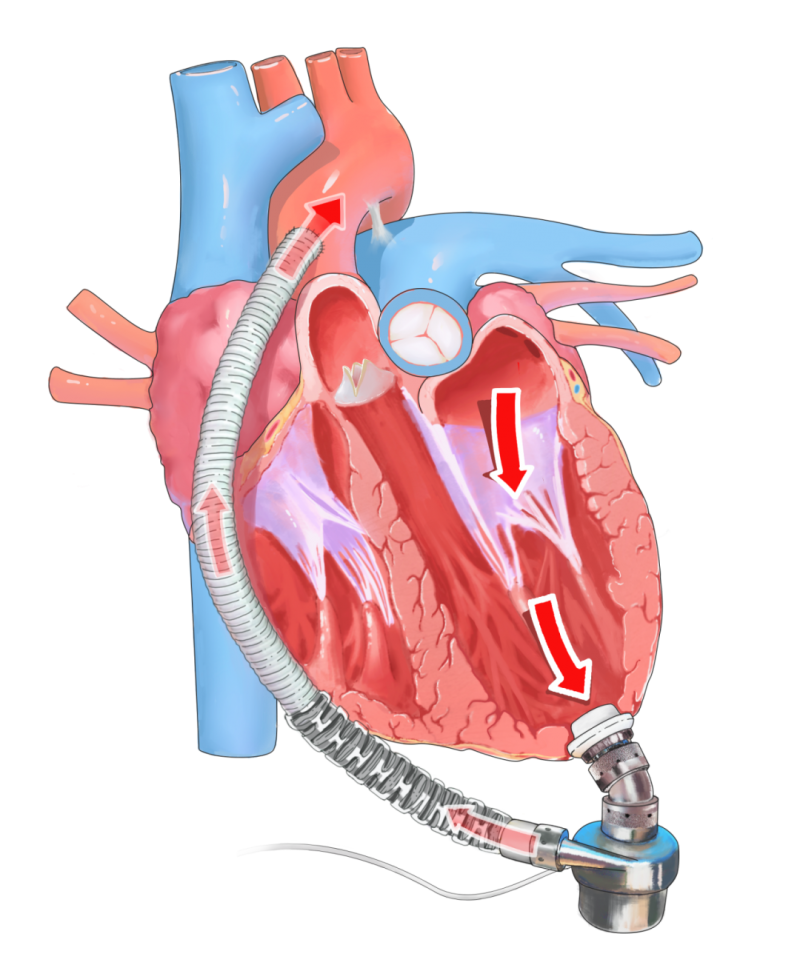
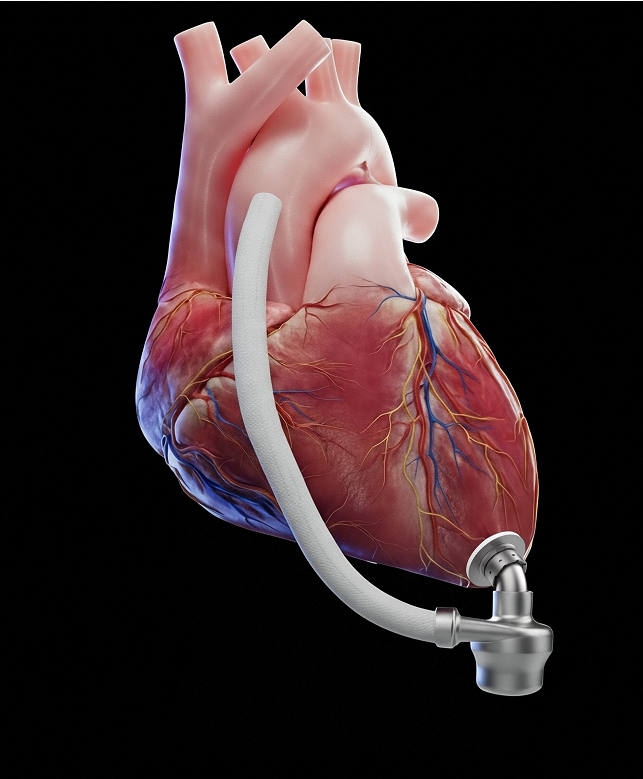
·瓣膜功能评估:经食道超声实时监测,二尖瓣反流从中量转为微量,三尖瓣反流降至微量,无需额外瓣膜干预。
·术中监测与撤机:确认LVAD位置理想,血流动力学参数稳定(CO 3.9L/min,CI 2.2L/(min·m2))。
术后管理与转归
术后早期管理(术后1-35天)
循环管理:术后初始起搏心率90次/分,平均血压72mmHg,中心静脉压5mmHg,肺动脉压30/46mmHg;因右心功能较差,予一氧化氮吸入联合安立生坦、西地那非降肺压,术后2周停用一氧化氮;术后第1天拔除气管插管,逐步停用血管活性药物。
抗凝与感染防控:术后予华法林联合阿司匹林抗凝,目标INR 2.0-3.0;术后出现体温及血象升高,予美罗培南抗感染,术后2周降级为头孢他啶,3周后停用,无感染并发症。
康复进程:术后第1天启动肠内营养,逐步开展康复训练;心功能、肾功能持续改善,术后35天顺利出院。
远期转归
术后5个月随访(2025年9月):左室舒张末径稳定在57mm,LVEF从26%提升至40%;右心功能显著改善(TAPSE 20mm,FAC 42%);NT-ProBNP降至1000pg/ml左右并维持稳定;肾功能基本恢复正常;患者已完全恢复日常活动,生活质量显著提升。
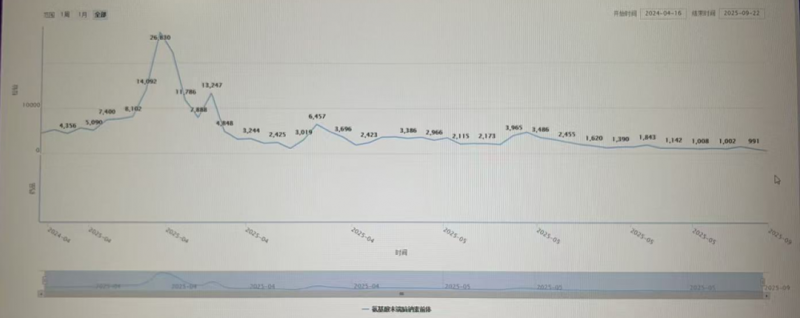

(图左:术后NT-proBNP变化;图右:术后随访患者已完全恢复正常生活)
阜外医院EVAHEART长期应用数据
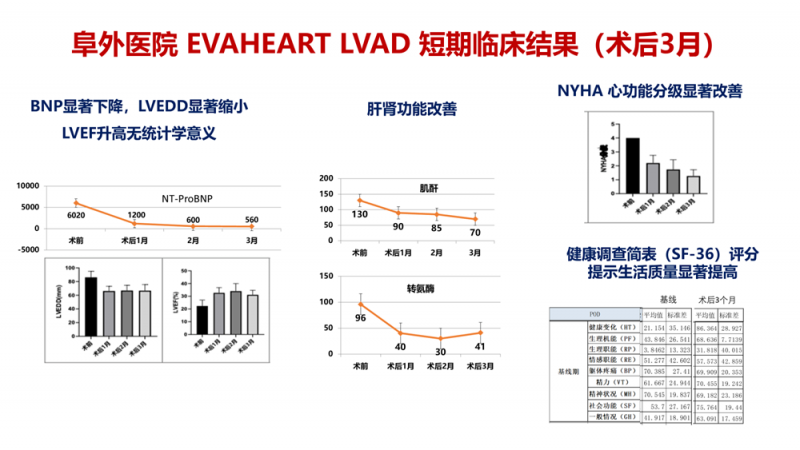
最后,陈凯医生也分享了阜外医院应用EVAHEART的经验,阜外医院EVAHEART LVAD植入术后3个月的随访数据显示,患者生物标志物和器官功能显著改善:BNP从6020 pg/ml降至560 pg/ml,LVEDD从63mm缩小至56mm;肝肾功能指标(肌酐、谷丙转氨酶、谷草转氨酶)持续改善;NYHA心功能分级从IV级显著改善至I-II级;SF-36生活质量评分各维度明显提升,表明患者日常生活能力和生活质量得到显著改善,充分验证了EVAHEART装置的临床效果。
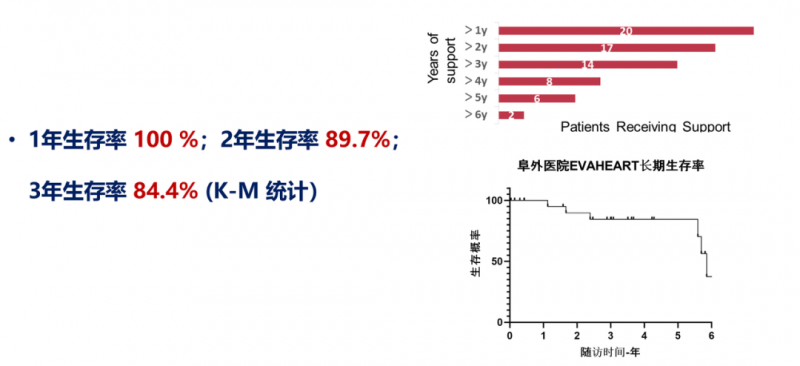
长期随访数据显示,1年生存率达100%,2年生存率89.7%,显著高于国际同类产品。
专家讨论
姜晓晓教授
大连医科大学附属第一医院

姜晓晓:小左室合并右心功能不良患者,LVAD植入的关键决策依据是什么?

陈凯:这类患者的核心决策依据在于精准评估右心功能不全的病因。本例通过漂浮导管检查明确右心功能差是继发于左心负荷过重和肺高压,而非原发性右心病变,预测左心泄压后右心功能可改善,这是手术的核心前提。其次,选择合适的LVAD装置至关重要,EVA-Pulsar?的无插入血管设计可避免抽吸室间隔,适合小左室患者,能减少右心衰和心律失常风险。此外,术前优化脏器功能、患者良好的依从性和家庭支持也是决策的重要考量。
龚达教授
北京大学第一医院

龚达:对于二尖瓣中大量反流的LVAD候选患者,如何决定是否同期行瓣膜手术?

陈凯:多数心衰患者的瓣膜反流是心室扩大继发引起的功能性反流。若瓣膜形态结构尚可,LVAD植入后左室负荷减轻,瓣膜反流多可显著改善。本例患者术前二尖瓣中大量反流,术后转为微量,就是典型例证。仅当存在瓣膜器质性病变(如二尖瓣狭窄、风湿性病变)或术后反流持续影响血流动力学时,才考虑同期行瓣膜成型或置换术。三尖瓣处理同理,中量以下反流可通过术后容量调节和右心功能改善缓解。
赵鸿教授
北京大学第三医院

赵鸿:右心功能不良患者术后远期,有哪些关键预防措施?

陈凯:术后远期预防的核心是动态监测心功能变化。扩心病等基础疾病可能进展,需定期复查超声心动图和NT-ProBNP,若出现右心功能恶化迹象,及时调整药物治疗。其次,严格遵循抗凝方案,避免血栓形成影响LVAD功能;控制感染风险,预防肺部感染诱发右心衰;同时注重患者生活方式管理,避免过度劳累和容量负荷过重。对于基因阳性的扩心病患者,还需长期监测心律失常风险。
学术拓展
本例患者左室偏小(LVEDD仅63mm),传统有插管式LVAD易引发进流导管吸取室间隔、形成室间隔缺损等并发症。EVA-Pulsar?的无插管式设计通过在心尖处建立进流通道,有效规避了这一风险。
其次,患者右心功能严重受损(TAPSE 11mm,FAC 16.6%),采用脉动血流设计的LVAD相比传统连续流装置,能产生近似生理性的搏动血流,更好地保护主动脉瓣功能,减少对右心的不利影响,促进原生右心功能恢复,这在右心差的患者中特别重要。
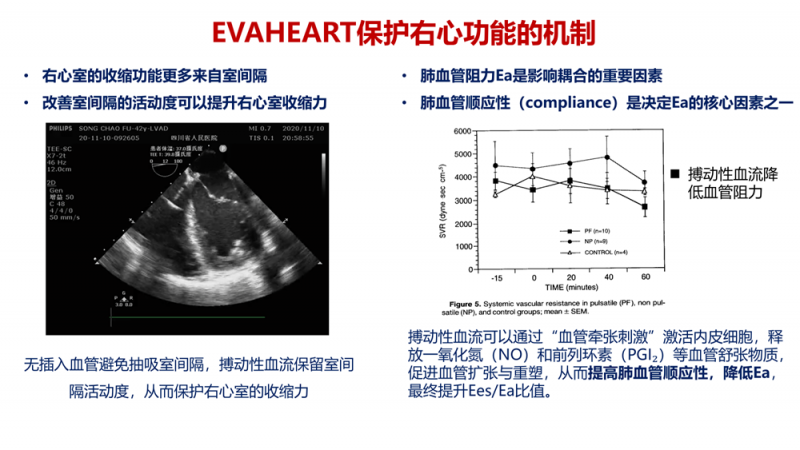
本例患者通过漂浮导管检查明确肺高压源于左心前负荷过重而非原发性肺血管疾病,这一发现是实施LVAD手术的关键前提。左心减负后肺循环和右心功能的改善,充分验证了这一治疗策略的科学性。术前充分的脏器功能优化和患者良好的依从性,为手术创造了最优条件;术后通过肺血管扩张剂的个体化应用和精细的血流动力学管理,支持了原生右心功能的逆向重塑。
关于瓣膜反流的处理原则:多数心衰患者的瓣膜反流是心室扩大继发引起的功能性反流。本例患者术前二尖瓣中大量反流,但瓣膜形态结构尚可,LVAD植入后左室负荷减轻,瓣膜反流即刻显著改善,证实了这一原则。仅当存在瓣膜器质性病变或LVAD植入后反流仍然严重时,才考虑同期行瓣膜干预。
长期LVAD支持中,脉动血流对原生心脏的保护作用值得关注。本例患者术后5个月LVEF从27%恢复至40%,右心功能也显著改善,这表明充分的左心减负、优化的血流动力学和脉动血流的保护作用,可能为原生心脏功能的逆向重塑创造条件,为后续可能的心脏恢复提供了希望。
结语
本例患者的成功救治充分展现了LVAD在复杂终末期心衰中的卓越价值。通过精准的血流动力学评估、科学的装置选择、充分的术前优化和精细化的术后管理,挑战“小左室+右心功能不良”的高难度手术并获得成功,实现了患者从濒危状态到完全康复的华丽蜕变。该病例为同类复杂心衰患者的诊治提供了重要参考。
郑重声明:此文内容为本网站转载企业宣传资讯,目的在于传播更多信息,与本站立场无关。仅供读者参考,并请自行核实相关内容。










